不同的物质有着不同的溶解度,而且即使是同一物质,它的溶解度大小也会因为各种而样的因素发生变化。
方法/步骤
-
1
当溶液为该温度下的饱和溶液时,可以比较该温度下,两种溶液的溶质质量分数大小比较不同溶液在该温度下的溶解度大小。
-
2
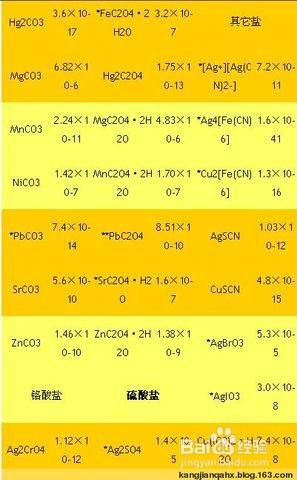
大部分固体溶解度随温度的上升而上升对于我们常见的沉淀,可以通过查阅资料比较各种物质的Ksp常数,叫溶度积常数,常数越大,溶解度越小.
-
3
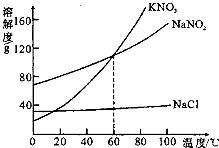
可以根据溶解度曲线来比较。
1.溶解度曲线上的每一个点表示溶质在某一温度下的溶解度。此时,溶液必定是饱和溶液。
2.在溶解度曲线的下方的点,表示该温度下的溶液是该物质的不饱和溶液。
3.在溶解度曲线上方的点,表示该温度下的溶液是该物质的过饱和溶液,也就是说,在溶液中存在未溶解的溶质。
-
4
还可以根据一些常见的溶解度口诀进行判断。
钾钠铵盐皆可溶 硝酸盐如水影无踪
盐酸盐不溶氯化银 硫酸盐不溶硫酸钙
碳酸盐只溶钾钠铵 溶碱有四位钾钠铵和钡
(酸式盐一般都可溶)
END
经验内容仅供参考,如果您需解决具体问题(尤其法律、医学等领域),建议您详细咨询相关领域专业人士。
作者声明:本篇经验系本人依照真实经历原创,未经许可,谢绝转载。
展开阅读全部
文章评论